Большое преимущество получает тот, кто достаточно рано сделал ошибки, на которых можно учиться.
Уинстон Черчилль
После долгих усилий всего коллектива приходит момент, когда мы можем смело сказать – мы создали систему управления качеством медицинских услуг в нашей клинике. Но как удостовериться, что ежедневные повторяющиеся процессы работают именно так, как это принято в организации, как это утверждено документами, как это должно работать? Как удостовериться, что новые сотрудники выполняют свою работу не так, как это им удобно или как они сами придумали, а в соответствие с регламентирующими документами?
Как найти ошибки и отрицательные примеры, на которых можно учиться и обучать вновь принятый персонал? Как обнаружить имеющиеся ошибки в процессах, когда они еще не успели привести к определенным последствиям?
Существует один единственный способ – аудит процессов системы менеджмента качества (СМК). И чем раньше мы начнем проводить аудит процессов, которые мы прописали, тем более своевременно: мы начнем устранять ошибки и совершенствовать созданную нами СМК, у нас появится возможность приступить к работе над ошибками и использовать данное преимущество в дальнейшем.
Основные положения внутреннего аудита
Аудит — это систематический, независимый и документированный процесс получения свидетельств в форме наблюдений и их объективной оценки с целью определения степени выполнения требований ISO 9001:2008, государственных регламентов, внутренних стандартов предприятия, а также с целью оценки эффективности работы подразделения.
Целями аудита являются:
- установление соответствия или несоответствия элементов системы установленным требованиям;
- определение эффективности СМК в подразделении; определение уровня соответствия стандартам и процедурам;
- проверка качества предоставления услуги;
- своевременное обнаружение и контроль проблем в подразделении;
- обеспечение обратной связи для корректирующих мероприятий, направленных на совершенствование действующей СМК в подразделении.
Под несоответствиями следует понимать невыполнение требований ISO 9001:2008, государственных регламентов, а также внутренних стандартов предприятия.Несоответствия бывают существенные и несущественные. Под несущественными несоответствиями понимают небольшое отклонение от установленных требований. Под существенными несоответствиями понимают невыполнение любого из пунктов стандарта.
Найденные несоответствия являются потенциалом для улучшения системы с помощью корректирующих и предупреждающих действий.
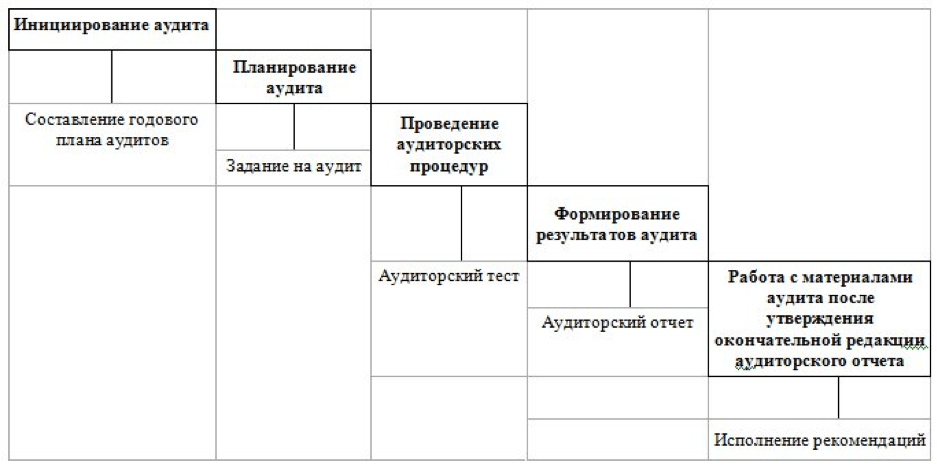
Этапы проведения внутренней аудиторской проверки представлены на рисунке 1.
Рис. 1. Этапы проведения внутренней аудиторской проверки
Подготовка документов
Для проведения аудита необходимо наличие следующих документов: план аудитов на текущий год; план проведения аудита конкретного подразделения (контрольный лист) с указанием следующих пунктов: наименование подразделения,цель и задачи аудита, список аудиторской группы, дата и место проведения аудита, перечень документов, на соответствие которым проводится аудит, перечень контрольных вопросов, список должностных лиц, которым должны быть направлены копии отчета об аудите.
Видеофиксация
При проведении аудита возможно использование фотоаппарата.
Наличие фотоаппарата является преимуществом, так как только видеофиксация позволит нам довести масштаб «беспорядка» до конечного потребителя продукта аудита (как правило, руководителя). Видеофиксация помогает также избежать фальсификации и субъективизма. Фотографии нарушений с комментариями вставляются в отчет об аудите. При проведении повторного аудита по результатам корректирующих мероприятий фотографии, расположенные в отчете, являются определяющим наглядным фактором (рис. 2).
Рис. 2. Пример фрагмента отчета по аудиту

Процедура аудита
Процесс проведения аудита включает в себя три стадии:
- Предварительную проверку документации.
- Проверку на месте.
- Составление отчета по аудиту.
Предварительная проверка документации
Системная документация по обеспечению качества, по возможности, проверяется в полном объеме. До проведения основного аудита аудитор может запросить основную документацию для предварительного изучения. Сертификационные аудиты всегда проводятся с запросом основных документов в электронном виде. При этом с аудитором подписывается соглашение о конфиденциальности.Проводится анализ результатов предшествующих аудитов. Основное внимание уделяется не только несоответствиям, но и корректирующим мерам и отметкам об их выполнении.Аудит в виде схемы представлен на рисунке 3.
Рис. 3. Схема проведения аудита СМК
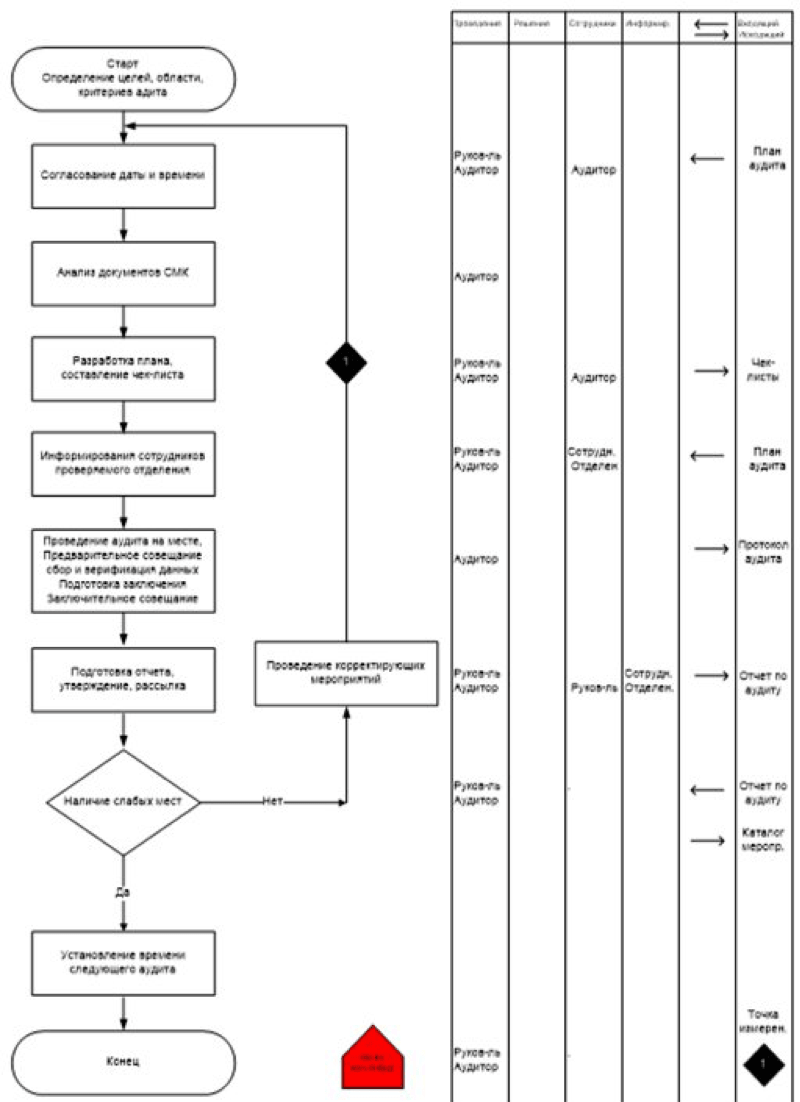
Проверка на месте
Проверка на месте включает в себя: Вводную беседу: сотрудникам подразделения поясняются цели и задачи проводимого аудита; выбираются определенные документы и элементы для более детального рассмотрения в ходе аудита. Аудитные беседы с отдельными сотрудниками на их рабочих местах:проверяются предположения, сделанные при работе с документами и определяются объекты для выборочных проверок; вопросы по аудиту задаются на основе контрольных перечней. Выборочные проверки, при которых проверяются: данные аудитных бесед, результаты предварительного изучения документов. Заключительную беседу, в ходе которой главный аудитор: подводит основные итоги проведенного аудита; дает обоснование оценок несоответствий.
- Основные пункты, на которые необходимо обратить внимание при проведении аудита: установление основных параметров состояния и деятельности аудитируемого подразделения; качественная оценка факторов риска, уровня соответствия стандартам; оценка возможности соблюдения технологических параметров; оценка системы внутреннего контроля; оценка качества предоставления услуги.
- Объективные доказательства несоответствия:основанная на фактах демонстрация различий между Руководством по качеству и связанными процедурами;основанная на фактах демонстрация различий между стандартами и реальным выполнением процесса.
Составление отчета по аудиту
- По завершении процедуры аудита составляется отчет (рис. 4), отражающий следующие моменты: обнаруженные несоответствия; решения о корректирующих действиях; назначение ответственных за исправление несоответствий; установление сроков исправления несоответствий.
После реализации корректирующих действий, руководитель аудитируемого подразделения информирует главного аудитора для последующего инспекционного контроля, о чем делаются дополнительные отметки в протоколе о несоответствии (отчете по аудиту).
Рис. 4. Пример отчета по аудиту
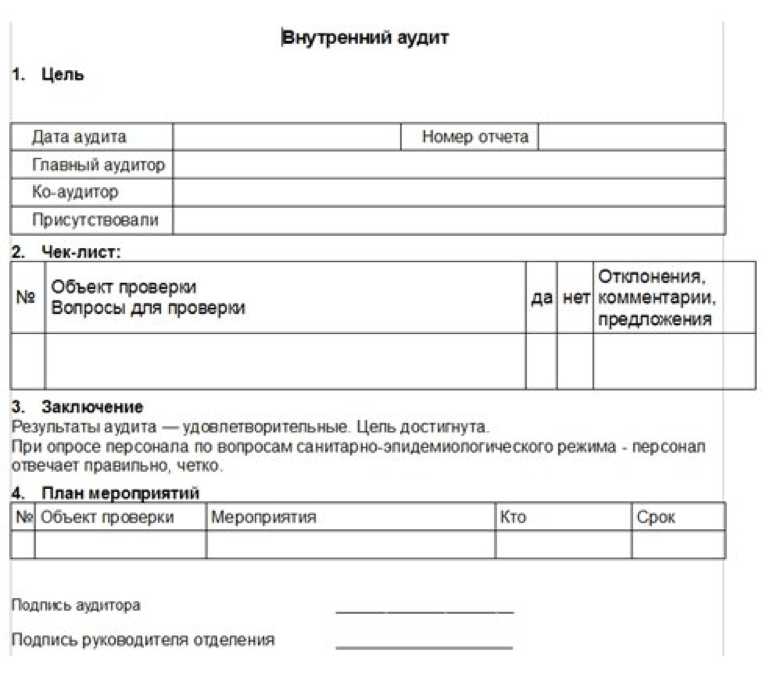
Анализ полученных результатов
Результаты аудита (с учетом мер по устранению несоответствий) служат основой для регулярного анализа, оценки состояния и определения эффективности системы качества руководством организации. Сводная информация о результатах аудитов, проведенных в течение года, попадает в ежегодный обзор системы управления на предприятии (менеджмент ревью). О составлении подобных отчетов мы расскажем в одном из следующих номеров.
- Однако проведение аудита не является самоцелью. Наша основная задача — найти ошибки и исправить их. Для этой цели существует процедура проведения корректирующих мероприятий. Эта процедура регламентирует порядок:анализа несоответствий, оценки необходимости разработки, внедрения и проверки эффективности корректирующих действий в подразделениях.
Словарь терминов
Так как язык СМК достаточно своеобразен, то необходимо определиться со словарем терминов, которые мы будем использовать. Для проведения корректирующих процедур в медицинском учреждении это приобретает особую значимость, оценить которую вы сможете, ознакомившись со словарем ниже:
Продукция – результат процесса, услуга (согласитесь, называть медицинскую услугу «продукцией» совсем непривычно, но с экономической точки зрения именно так она и называется).
Несоответствующая продукция – продукция, неудовлетворяющая требованиям нормативной документации (простым языком – медицинская услуга плохого качества).
Корректирующее действие – действие, предпринятое для устранения причины обнаруженного несоответствия или другой нежелательной ситуации. У несоответствия может быть несколько причин.
- Нельзя путать понятия «корректирующее действие» и «предупреждающее действие»: корректирующее действие предпринимается для предотвращения повторного возникновения события;
- предупреждающее действие предпринимается для предотвращения возникновения события.
Разрешение на отступление – разрешение на отступление от исходных установленных требований к продукции до ее производства, как правило, дается на ограниченное количество продукции или период времени, а также для конкретного использования. Напоминаю, в нашем случае продукция — это медицинская услуга. Примером отступления могут быть подготовительные мероприятия в экстренных ситуациях, например, когда действовать надо немедленно. Такие отступления необходимо прописывать в стандартных операционных процедурах.
Выпуск — разрешение на переход к следующей стадии процесса.К пяти составным частям процесса, которые можно, по необходимости, разбить на более мелкие, относятся:
Материалы — основные и вспомогательные. Все материалы должны иметь: сопроводительную документацию установленной формы в виде паспорта или сертификата; должностные и рабочие инструкции с указаниями по проведению проверки и методов проверки соответствия материалов установленным требованиям.
- Оборудование — технологическое, контрольно-измерительное, приспособления, инструменты, компьютеры и программное обеспечение. В должностные и рабочие инструкции должны быть внесены требования по регулярной проверке пригодности оборудования для выполнения процесса.
- Среда — температура, влажность, уборка помещений, кондиционеры. В должностные и рабочие инструкции должны быть внесены требования по регулярной проверке соответствия среды заданным параметрам.
- Персонал — обученные и аттестованные сотрудники, подчиняющиеся собственнику процесса. Для всех видов работ, входящих в процесс, должны быть указаны физические и профессиональные требования.
- Технология — документированный порядок выполнения работ, входящих в данный процесс, в том числе краткие выписки из документации, находящиеся на рабочих местах.
Корректирующие мероприятия
Началом для разработки корректирующих действий (КД) является документально зафиксированное отклонение, несоответствующее установленным критериям.
- Нормы и критерии, по которым принимается решение о разработке КД, должны охватывать:рекомендации, претензии, жалобы и рекламации потребителя; результаты внутреннего аудита; показатели процесса; несоответствие продукции установленным нормам; информацию о наличии и частоте возникновения аналогичных отклонений.
На рисунке 5 – схема проведения корректирующих мероприятий.
Рис. 5. Проведение корректирующих мероприятий: КД – корректирующие действия, РП –руководитель подразделения, ГВ – главный врач, От – ответственный, АО – анализ отклонений
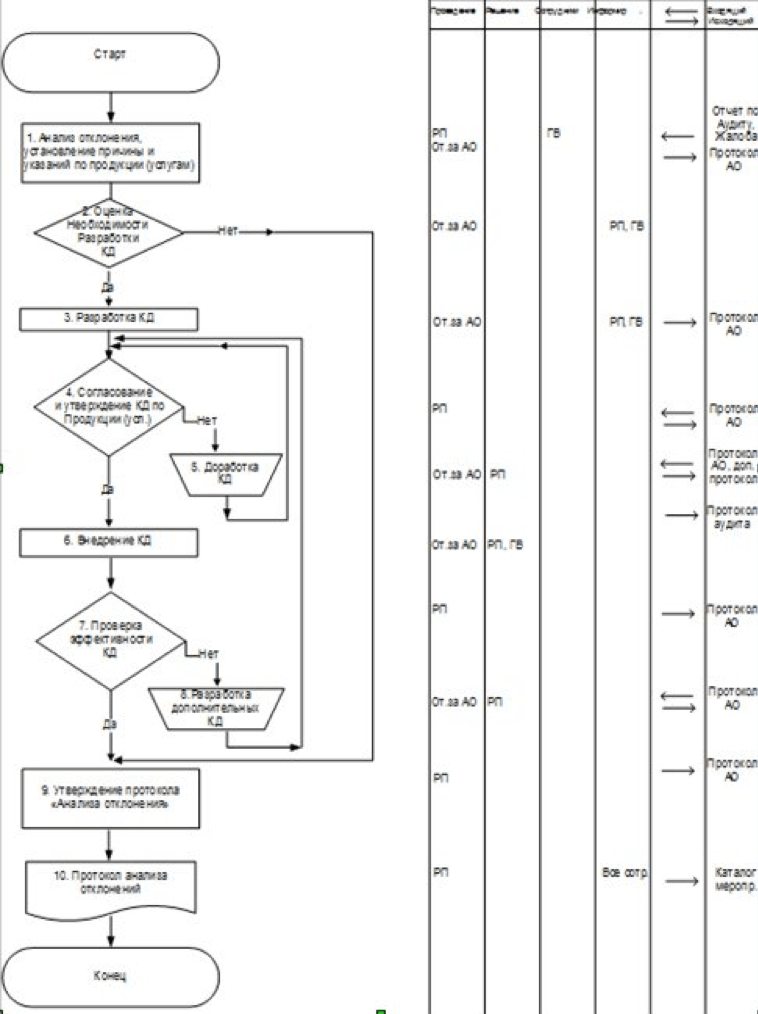
К элементу 1:
- Ответственного за анализ обычно назначает руководитель подразделения (РП). РП может и сам выступать в роли ответственного за проверку, анализ и др. При проведении анализа ответственный может обратиться в любое подразделение и получить необходимую помощь. Результат анализа отклонений (АО) оформляется в «Протоколе анализа отклонения» (рис. 6) (далее – протокол) по форме, указанной в приложении 1:В п. 2. протокола заносится причина отклонения, установленная по результатам анализа.П. 3 протокола заполняется в случае, если отклонение касается медицинской услуги или ее сервисной составляющей. В него ответственный за анализ заносит предложения по действиям с услугой, произведенной с отклонениями от норм или условий клиники. Этот пункт вступает в силу после согласования и утверждения «Указаний по продукции» в п. 5 протокола.В п. 4 протокола заносится заключение ответственного за анализ отклонения о целесообразности разработки и внедрения КД.Протокол должен иметь согласующие подписи руководителя подразделения-виновника отклонения и утверждающую подпись РП собственника процесса.
- Если отклонение затрагивает качество оказанных медицинских услуг, то обязательно согласование с главным врачом (ГВ) и РП. Если ответственный за АО сделал заключение о нецелесообразности разработки КД, то проверку этого заключения проводит начальник подразделения при утверждении протокола. При этом ответственность за АО и разработку КД может быть возложена только на одно лицо.
К элементам 2, 3:
- При разработке корректирующих мероприятий ответственный за разработку (РП) в первую очередь проверяет оценку:необходимости КД, адекватность затрат на КД,тяжести отклонения.Результат оценки заносится им в п. 4 протокола.
К элементам 4, 5:
- Протокол должен иметь согласующие подписи РП, которые принимают участие во внедрении КД, и утверждающую подпись начальника подразделения собственника процесса.
- В случае отсутствия согласия участников с предложенными КД, вопрос выносится на общего руководителя обоих начальников подразделений. Руководитель, утверждающий КД, должен проверить наличие согласования со всеми заинтересованными лицами. При доработке КД, ответственный за их разработку и внедрение может выбрать один из двух способов: оформить дополнительный протокол в виде приложения к основному; переоформить протокол заново с внесением изменений только в п. 4. Если действия затрагивают качество оказанной услуги, то обязательно согласование с ГВ и РП. ГВ и РП проверяют характер и степень влияния разработанных действий на качество оказания медицинской услуги.
- Если ответственный за АО сделал заключение о нецелесообразности разработки КД, то проверку этого заключения проводит РП при утверждении протокола.
К элементу 6:
- Реализация КД производится ответственными, назначенными в п. 5 протокола. Контроль за своевременностью и полнотой выполнения КД возлагается на ответственного за их разработку.
К элементу 7:
- Проверку эффективности КД производит ответственный за проверку. Способ проверки указывается в п. 6 протокола.
- Результат проверки ответственный за проверку заносит в п.п. 7, 8 протокола.
К элементу 8:
- В случае если причина несоответствия не устранена, ответственный за проверку: заполняет п.п. 7, 8, совместно с ответственным за разработку и внедрение КД, производит разработку дополнительных КД по устранению причины несоответствия, в п. 1 «Исходная информация» протокола дополнительно указывается «неэффективность корректирующих действий». Возможна ситуация, когда затраты на дополнительные КД неадекватны тяжести отклонения. В этом случае: в п. 8 протокола делается отметка, протокол передается РП для утверждения.
К элементу 10:
- В случае если причина несоответствия устранена, ответственный за проверку: заполняет п.п. 7, 8, передает протокол РП на утверждение. Утвержденный отчет с заключением об устранении причин несоответствия является документом (записью по качеству), подтверждающим завершение работы по устранению причины несоответствия.
Необходимым элементом является описание документирования и архивирования процедуры в форме простой таблицы (см. рис. 6). Протокол рассылается в заинтересованные подразделения, например, в отдел качества.
Рис. 6. Образец протокола анализа отклонений

Все это выглядит на первый взгляд достаточно сложно, но на самом деле СМК создается такой, какой она удобна для конкретного медицинского учреждения в зависимости от количества подразделений, персонала, оказываемых услуг и т. д., т. е. в зависимости от индивидуальных условий и потребностей. Стоит попробовать один раз, чтобы убрать лишние, непонятные или ненужные шаги, и таким образом сделать данную систему оптимальной. Тогда система аудитов и корректирующих мероприятий станет не трудной обязанностью, а интересным источником оптимизации работы всего учреждения.
Журнал «Консилиум главных врачей», № 4 (16) / 2013