Исследования показывают, что самые грязные в микробиологическом плане – общие полотенца в ординаторских и сестринских, телефоны, в том числе мобильные, стетоскопы, клавиатуры и компьютерные мыши.
Стоит в отделение попасть пациенту с синегнойной инфекцией, которого не изолировали, руки после которого не помыли, либо помыли без мыла, вытерли общим полотенцем и пошли смотреть других пациентов, к вечеру обсеменению подвергнутся весь персонал отделения, все пациенты и все доступные поверхности.
В данной статье мы продолжим разговор о внутрибольничных возбудителях инфекций, связанных с медицинскими вмешательствами, и о путях решения проблем, возникающих с ними.
Начнем с так называемого инфекционного контроля, поскольку, как показывает опыт, только при должном внимании и вмешательстве администрации удается наладить его в должной мере и позволяет в дальнейшем экономить существенные денежные средства.
Необходимость проведения инфекционного контроля
Для начала нужно понять, зачем вообще нужны программы инфекционного контроля, ибо, казалось бы, должно хватить мер, связанных с санитарно-эпидемиологическим режимом. Дело в том, что никаких санитарно-эпидемиологических мероприятий не хватит, если в лечебном учреждении не налажены рациональная антибактериальная терапия и элементарные мероприятия по недопущению возникновения и распространения вспышек нозокомиальных инфекций, что невозможно сделать без постоянного микробиологического мониторинга. И, что самое главное для любого организатора здравоохранения, – если не наладить работу по инфекционному контролю, то каждый год вы будете иметь все большие затраты на антибактериальную терапию при сохраняющемся низком ее качестве, увеличении сроков госпитализации и использования дорогостоящих методик оказания медицинской помощи. То есть лечебное учреждение, не наладившее данный раздел, постоянно работает себе в убыток.
Напомним, что первыми под удар попали препараты группы бета-лактамов. Исторически так сложилось, что микробы в первую очередь научились защищаться от них с помощью ферментов – бета-лактамаз. Люди придумали цефалоспорины, микробы ответили бета-лактамазами расширенного спектра. Люди создали карбваенемы – микробы в своей эволюции отбились карбапенемазами. А ведь бета-лактамы до сих пор являются самыми безопасными из всех групп антибактериальных препаратов и относительно доступны в финансовом плане на фоне вновь выводимых на рынок препаратов, где ценник за упаковку давно перешагнул сумму в 20 тысяч рублей. Кроме прямых финансовых потерь, «распоясавшиеся микробы» в первую очередь угрожают результатам проводимых в лечебном учреждении манипуляций, будь то хирургическое лечение, в том числе и высокотехнологическое, либо лечение, связанное с социально важными заболеваниями. Если к таким пациентам «прицепится» нозокомиальная микрофлора и разовьется инфекция, связанная с медицинским вмешательством, мало того, что будут потеряны результаты уже проведенного оперативного лечения (придется удалять инфицированный клапан, протез и т.п.), но и есть большой риск потерять самого пациента. Про финансовую сторону даже упоминать не стоит, ибо убытки будут колоссальными.
Решением проблемы, как уже говорилось выше, будут мероприятия по внедрению принципов инфекционного контроля. Остановимся на основных этапах инфекционного контроля в условиях стационара.
Этапы инфекционного контроля в стационаре
Первое и самое главное, что надо сделать, – это выявить, с чем же именно предстоит иметь дело, то есть необходимо изучить микробный пейзаж отделений лечебного учреждения. Для этого проводятся два вида микробиологического мониторинга – текущий и направленный.
Текущий мониторинг позволяет:
- выявить патогенов, живущих в отделениях;
- выявить у них тенденции развития антибиотикорезистентности;
- оценить эффективность уже проводимых санитарно-эпидемиологических мероприятий;
- планировать стратегию инфекционного контроля на будущее.
Этот вид мониторинга носит ретроспективный характер и эффективен только в том случае, если на основании его данных проводится работа, позволяющая изменить ситуацию в стационаре, поэтому заниматься им должна специально подобранная команда специалистов, а не энтузиаст-одиночка. К сожалению, это как раз тот случай, когда «один в поле не воин».
Второй вид мониторинга, направленный мониторинг, проводится рутинно и ежедневно с целью выявить возможную вспышку нозокомиальных инфекции или фиксировать каждый отдельный случай. Он требует намного меньших затрат, его результаты видны мгновенно, и, самое главное, он позволяет обучить и натренировать персонал на действия, необходимые при обнаружении внутрибольничной инфекции в максимально короткие сроки.
Если текущий мониторинг должен проводиться изо дня в день и годами с привлечением к работе группы специально обученных специалистов, то в направленном мониторинге участвуют все сотрудники отделения, в котором выявлен случай развития инфекции (или локальная вспышка), и он заканчивается после проведения всех необходимых мероприятий и расследования результатов произошедшего.
Мероприятия в рамках инфекционного контроля
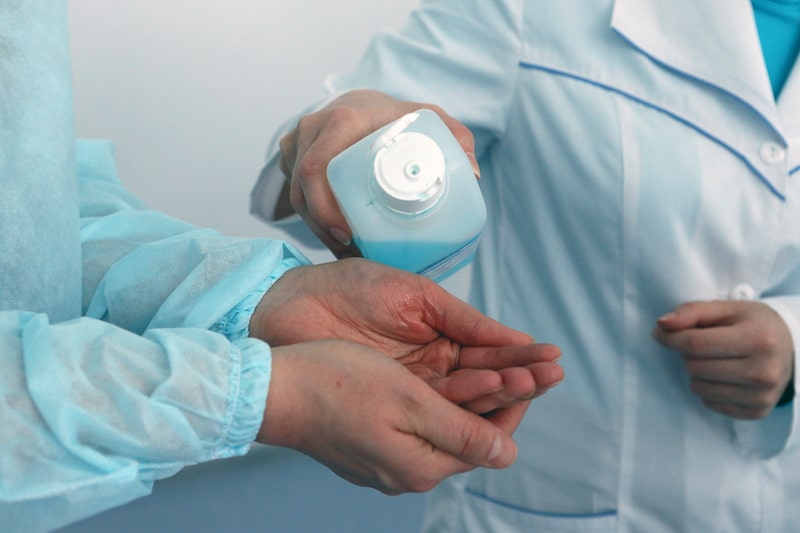
Мытье рук
Первое, самое главное, но при этом самое простое – это мытье рук. Именно на руках в большинстве случаев мы переносим возбудителей от одного пациента к другому. На них же мы несем нозокомиальных возбудителей к себе домой. С рук идет обсеменение всего окружающего пространства. Проведенные исследования показывают, что самые грязные в микробиологическом плане – это общие полотенца в ординаторских и сестринских, телефоны, в том числе и мобильные, стетоскопы, клавиатуры и компьютерные мыши.
Руки плохо моют везде в мире – не только в России. А ведь давно известный факт, что мытье рук с мылом в течение 10 секунд приводит к удалению с поверхности кожи практически всех транзиторных грам-отрицательных бактерий (Руководство по инфекционному контролю в стационаре, 2003 г). Те же данные получены и при применении современных антисептиков.
Руки необходимо обрабатывать после каждого пациента, и это особенно актуально для пациентов, находящихся в отделениях реанимации и интенсивной терапии. Скажем больше, руки должны обрабатываться после каждого контакта с контаминированной раной и перед манипуляциями на неконтаминированных участках у одного и того же пациента (например, при работе с сосудистым катетером). Что же происходит на самом деле – по данным ISID, приверженность к мытью рук составляет не более 40% в отделениях ОРИТ и еще ниже в других отделениях. По России таких данных нет, но есть обоснованные подозрения, что они будут намного хуже.
Смена перчаток
Еще одна проблема в том, что наш персонал полностью уповает на перчатки. Сняли перчатки, надели новые, и считается, что проблема решена. А ведь ношение перчаток никак не отменяет обработки рук, то есть сняли перчатки – обработали руки – надели новые перчатки – только после этого подошли к следующему пациенту.
Изоляция инфицированных пациентов
Следующее важное и наиболее эффективное мероприятие – это изоляция пациентов с подозреваемым или выявленным инфекционным заболеванием, связанным или не связанным с оказанием медицинской помощи. Изоляция может быть как в отдельную палату, так и в специально оборудованный бокс изолятора. Цель этого мероприятия – максимально ограничить распространение инфекции как от пациента к пациенту, так и от пациента к медицинскому персоналу отделения.
Как показывают опыт и многочисленные исследования, пациентов изолируют еще хуже, чем моют руки. В результате этого, стоит в отделение попасть одному пациенту с синегнойной инфекцией, которого не изолировали, руки после которого не помыли, либо помыли без мыла и вытерли общим полотенцем и пошли смотреть других пациентов, к вечеру обсеменению синегнойкой подвергнутся весь персонал отделения, все пациенты и все доступные поверхности. Очаг для вспышки этого вида инфекции готов.
Таким образом, подозрительных в инфекционном плане пациентов необходимо изолировать от всех остальных. Далее, в отношении него должны вступить в силу стандартные меры предосторожности.
- Необходимо мыть руки после каждого контакта с пациентом вне зависимости от наличия перчаток.
- Перчатки для работы с такой категорией пациентов должны быть в наличии в достаточном количестве, а не, как мы привыкли, в сильно урезанном варианте.
- При выполнении процедур, связанных с контактом с биологическими жидкостями, необходимо использовать маски и защитные очки.
- Перед входом в изолятор должны быть приготовлены отдельный, максимально закрывающий повседневную медицинскую одежду халат и бахилы. После манипуляций с пациентом они должны быть сняты и оставлены на территории изолятора. Отправляться на обработку они должны вместе с другим бельем из изолятора, не смешиваясь с другим бельем отделения. Мешки для инфицированного белья должны быть отдельными и надежно запакованными, чтобы избежать контакта инфицированного белья с чистым, в микробиологическом плане, бельем.
- Изоляторы должны обрабатываться соответствующим образом, с применением соответствующих методов дезинфекции.
- Перемещения пациента по стационару следует ограничить минимально необходимым пространством. В идеале методы диагностики должны «идти» к такому пациенту, а не пациент доставляться к ним.
- После того как пациент покинет изолятор, там должна быть проведена заключительная дезинфекция.
Казалось бы, все сложно, но это не так. Стоит пару раз «обкатать» эти мероприятия, и дальше все пойдет намного проще, особенно если весь персонал замотивирован на использование данных методов работы.
Реализация мероприятий на практике
Представим в общих чертах, как на практике может быть поставлена эта работа в стационаре. Итак, в стационаре появляется пациент, возможно угрожаемый по одной из потенциально опасных для наших отделений инфекций. С самого начала проводится своеобразная стратификация риска, и если риск высокий, то пациент будет максимально изолирован от всех остальных. Например, будет использован изолятор реанимационного отделения или отдельная палата, если реанимация не требуется, с соответствующими мерами санитарно-эпидемиологического режима. До начала антибактериальной терапии у пациента будет проведен забор всего необходимого для микробиологического исследования материала. Микробиологическая лаборатория оснащена автоматическим анализатором, что позволяет относительно быстро получать данные как по возбудителю, так и по антибиотикочувствительности. Кроме того, на начальном этапе врач может заказать мазок по Граму, чтобы быть ориентированным по имеющейся микрофлоре – грамположительной или грамотрицательной, что позволяет более корректно назначать эмпирическую антибактериальную терапию.
Если в процессе исследования микробиологи обнаружили «маячкового» возбудителя, помимо лечащего врача о нем оповещается эпидемиологическая служба и главная медицинская сестра, которые разворачивают соответствующие санитарно-эпидемиологические мероприятия и изолируют пациента, если это по каким-либо причинам не было сделано ранее. Далее, если требуется, приходит врач-клинический фармаколог, который совместно с лечащим врачом либо заведующим отделением согласовывает необходимую антибактериальную терапию. После того как пациент покидает стены изолятора, изолятор подвергается полной заключительной дезинфекции с использованием самых эффективных для нашей микрофлоры, дезинфицирующих средств, распыляемых специальными пушками, что позволяет обработать абсолютно все имеющиеся поверхности.
Результаты всей проведенной работы докладываются заместителю главного врача по лечебной работе, которая производит координацию действий всех служб.
Помимо вышеуказанного алгоритма в рамках текущего мониторинга в постоянном режиме проводятся посевы в отделениях, для того чтобы точно знать, что и где у нас летает и не требуется ли какой-либо дополнительной обработки. Кроме того, весь медицинский персонал обеспечен дезинфицирующими средствами для обработки рук, перчатками и одноразовыми наборами медицинской одежды для изоляторов. И все эти мероприятия позволяют эффективно противостоять распространению инфекции как внутри одного отделения, так и по стационару в целом.
Итак, все вышеуказанные мероприятия позволяют совершенно точно знать возбудителей и к чему они уже устойчивы, предпринимать определенные шаги, в том числе и в виде направленной антибактериальной терапии, для предотвращения появления новых механизмов резистентности, не допускать формирования и развития очагов таких инфекций, как синегнойная, стафилококковая и ацинетобактерная, что позволяет довольно долгое время не увеличивать количество денег, используемых на закупку антибактериальных препаратов и не рисковать результатами проводимых в стационаре высокотехнологичных манипуляций. Согласитесь, это весомая причина, чтобы заняться микробиологическим мониторингом и инфекционным надзором в собственном лечебном учреждении.
Микробиологическая лаборатория
Еще один вопрос, связанный с мониторингом, – заводить (или продолжать содержать уже имеющуюся) микробиологическую лабораторию или подписать договор со сторонней организацией. Ответим достаточно бескомпромиссно – микробиологическая лаборатория должна быть собственной. Да, мы еще далеки от западных стандартов, где микробиологи работают 24 часа в сутки, но даже в течение имеющегося рабочего дня работающая на территории лаборатория – это большое благо для всего ЛПУ, поскольку в любое время туда можно отправить на исследование материал, а не собирать его скопом и везти в строго указанный день к строго указанному времени в строго указанном количестве (опять же на транспортных средах некоторая экономия будет). А если количества не набирается, то и без того длительное микробиологическое исследование займет вообще катастрофическое количество времени, тогда как врачи будут продолжать менять антибиотики, ввергая больницу во все большие финансовые траты.
Еще одно преимущество, о котором постоянно забывают, – это окраска мазков по Граму. Недорогой, но абсолютно необходимый и, к сожалению, совершенно недооцененный метод исследования. А ведь именно он в течение часа дает ответ о принадлежности возбудителя к грам-положительным или грам-отрицательным, или мы вообще имеем дело с микст-инфекцией и нам будет необходима комбинация антибактериальных препаратов. В случае пациента с тяжелым течением заболевания этот нехитрый анализ в прямом смысле может спасти жизнь, так как в качестве стартовой эмпирической терапии ему с высокой долей вероятности будет назначен необходимый антибиотик, тем более что давно установлен тот факт, что максимально раннее начало антибактериальной терапии достоверно в разы снижает летальность.
И еще одно неоспоримое преимущество, связанное с микробиологическим мониторингом, – проще и дешевле это делать у себя, легче скоординировать все службы, образцы быстрее попадут в лабораторию, и с ними начнется вся необходимая работа, а также будет меньше разговоров по городу, что совсем немаловажно, так как мониторинг проводится для того, чтобы устранять ошибки или корректировать происходящее.
Список «маячковых возбудителей»
И в заключение еще немного практической информации.
У каждого лечебного учреждения должен быть свой список «маячковых возбудителей», за которыми необходимо наладить целенаправленное наблюдение.
К примеру, могут отслеживаться следующие возбудители.
- Klebsiella spp. Почему так необходимо пристально следить за этим возбудителем? Дело в том, что именно клебсиеллы являются чуть ли не основным источником карбапенемаз – ферментов, разрушающих всю группу бета-лактамов, включая карбапенемы. То есть если у нозокомиальной микрофлоры детектируются бета-лактамазы расширенного спектра, в нашем арсенале остаются карбапенемы; если же у нас завелись клебсиеллы с карбапенемазами – весь класс бета-лактамов для нас будет потерян. Более того, клебсиелла быстренько передаст свои карбапенемазы другой госпитальной микрофлоре, а дальше что делать? Если карбапенемазы еще не поселились в вашем стационаре, задача номер один – это не допустить их появления и предотвращать попытки формирования карбопенем-устойчивых штаммов. Для этого могут использоваться максимальные дозировки фторхинолонов или самих карбопенемов для предотвращения селекции устойчивых штаммов. На первый взгляд, это может показаться чрезвычайно затратным, но, как показывает опыт, мы третий год затраты на антибактериальную терапию не повышаются ни на копейку. Назначать эту терапию, как и оценивать риски может специально обученный человек в лице клинического фармаколога. У рядовых врачей доступа к препаратам резерва нет.
- Pseudomonas aeruginosa. Этот возбудитель должен мониториться везде, ибо последствия его приживления в стационаре ведут к катастрофическим финансовым и пациентским потерям. Синегнойки боятся все, в свое время ею достаточно серьезно запугали, и на тот период это было правильно – полирезистентная синегнойная палочка это практически воплощение абсолютного зла – если она детектирована у пациента, иной раз приходится стоять и смотреть, как пациент уходит, несмотря на все усилия по лечению и огромное количество вливаемых препаратов. Но есть одно «но», про которое либо не знают, либо забывают, либо просто не верят. С синегнойной палочкой достаточно просто справиться с помощью приведенных выше противоэпедемических мероприятий: пациентов изолировать, руки мыть, полотенца использовать одноразовые, дезинфекцию проводить только теми средствами, которые эффективны против живущего у вас штамма.
Если к вам залетает дикая синегнойка (а она достаточно прогнозируемая, если привозят политравму или ЧМТ с высокой степенью загрязнения), пациент отправляется в изоляцию и «в ружье» поднимается все отделение, куда такой пациент поступил. И никому лишний раз ничего говорить не надо – все знают, что этого возбудителя надо истребить. Дикая синегнойная палочка эрадицируется достаточно просто, главное – не дать ей выбраться из изолятора. После выписки пациента заключительной дезинфекции подвергается как сам изолятор, так и отделение, а потом еще несколько раз проводятся посевы всех доступных поверхностей на предмет, не выскочило ли что наружу. Кроме того, про данного возбудителя оповещаются все заинтересованные лица, и контроль усиливается по всему стационару (это и есть пример направленного мониторинга).
- Грибы. Включить грибы в маячковые необходимо, если вы имеете дело с онкологическими больными, а также с больными, имеющими ВИЧ. Современная противогрибковая терапия стоит столько, сколько не стоит антибактериальная терапия ни одной бактериальной инфекции, а потому лучше знать и не допускать на своей территории селекции особо устойчивых штаммов.
- S.aureus – необходимо мониторить на наличие/отсутствие MRSA штаммов. Кроме того, необходимо мониторить носительство MRSA среди медицинского персонала, так как он, как контаминат, спокойно существует в большинстве носоглоток персонала любого ЛПУ. Эрадицируется мупироцином, но об этом, как и о тактике лечения и о препаратах выбора, мы уже говорили ранее.
- Acinetobacter spp. – это тема для отдельного большого разговора.
- Clostridium difficille – и это тоже тема отдельного разговора.
Конечно, данный список должен быть дополнен вашими локальными возбудителями, которые ваш стационар будет мониторить в постоянном режиме и принимать соответствующие меры по недопущению распространения инфекций, связанных с медицинским вмешательством, что в конечном итоге приведет к значительной экономии финансовых ресурсов.
Подводя итоги, мы можем порекомендовать одно небольшое издание 2003 года «Руководство по инфекционному контролю в стационаре» международного общества по инфекционным болезням (ISID) и российские национальные рекомендации от 2012 года «Стратегия и тактика применения антимикробных средств в лечебных учреждениях России». В этих изданиях максимально подробно и доступно освещены те вопросы, которые были затронуты в статье.
Журнал «Консилиум главных врачей», № 3 (27) / 2014